Aluminiumchlorid
| Aluminiumchlorid. | |||||
   |
|||||
| Ausweis | |||||
|---|---|---|---|---|---|
| Name der Internationalen Union für reine und angewandte Chemie | Aluminiumtrichlorid | ||||
| Synonyme | Aluminiumchlorid | ||||
| CAS -Nummer | |||||
| Europäische Chemikalienagentur – Nichts | 100.028.371 | ||||
| Nr._CE | 231-208-1 | ||||
| RTECS_Nein | BD0525000 | ||||
| Flugsicherungscode | |||||
| Bob Kim | 24012 | ||||
| Er lächelte. |
[Zeigen]
|
||||
| hügel |
[Zeigen]
|
||||
| Aussehen | hellgelbe Volltonfarbe | ||||
| Chemische Eigenschaften | |||||
| Formel | AlCl3 [Isomere ] | ||||
| Molmasse 1 | 133341±0006 g/mol Aluminium 20,23%, Chlor 79,76%, |
||||
| Physikalische Eigenschaften | |||||
| Schmelzpunkt | 190 °C [ Siehe [optional] | ||||
| Siedepunkt | 182,7 °C , 752 mmHg (Standard) 2 | ||||
| Schmelzen | In Wasser: 439 g/l -1 ( 0 °C ), 449 g/l -1 ( 10 °C ), 458 g/l -1 ( 20 °C ), 466 g/l -1 ( 30 °C ), 473 g/l -1 ( 40 °C ), 481 g/l -1 ( 60 °C ), 486 g/l -1 ( 80 °C ), 490 g /l -1 ( 100 °C ). Ethanol: 1000 g / l -1 ( 12,5 °C ). Chloroform: 0,7 g/l -1 ( 20 °C ). CCl4: Lösung . Ether: Lösung [Zusätzlicher Link ] |
||||
| Schüttdichte | 2,44-2,48 g / cm32 | ||||
| Wendepunkt | 26,3 bar , 346,85 ° C | ||||
| Kristallographie | |||||
| Kristallsystem | monoklines System | ||||
| Bravis-Netzwerk | Zelle | ||||
| Zwei Pearson-Symbole | Maschine C 16 4 | ||||
| Kristallklasse oder Raumgruppe | C2/m ( Nummer 12 ) 4 | ||||
| Berichtsstruktur | D0 15 4 | ||||
| Vorbeugende Maßnahmen | |||||
| Singapur 5 | |||||
 Risiko H314 [+]
|
|||||
| NFPA 704-Standard | |||||
|
0
3
2
|
|||||
| Transport 2 | |||||
[+]
[+]
|
|||||
| Umwelttoxikologie | |||||
| DL 50 | 3450 mg/kg in 1 [ Variante. [optional] | ||||
|
|
|||||
| SI- und CNTP-Maßeinheiten, sofern nicht anders angegeben. | |||||
| Korrektor |
|||||
Aluminiumchlorid (AlCl3 ) , auch Aluminiumtrichlorid oder Aluminium(III)-chlorid genannt , ist ein Salz des Aluminiumchlorids. Die wasserfreie Form hat eine seltsame Struktur: Obwohl Halogenide Metalle mit einer hohen elektrischen Ladung sind, sind die chemischen Bindungen in ihnen überwiegend kovalenter Natur und nicht wie erwartet ionischer Natur. Dies führt dazu, dass AlCl3 einen niedrigeren Schmelz- und Sublimationspunkt hat (letzterer liegt bei 178 °C ) und im flüssigen Zustand im Gegensatz zu ionischen Halogeniden wie Natriumchlorid ein schlechter Stromleiter ist. Die Verbindung liegt im festen Zustand in Form eines hexagonalen Gitters vor. Es schmilzt und bildet das vierwertige Dimer Al2Cl6 , das verdampfen kann, sich jedoch bei höheren Temperaturen zu der BF3-ähnlichen Spezies AlCl3 zersetzt .
Aluminiumchlorid ist sehr verdünnt und kann bei Kontakt mit Wasser während der Hydratisierung explodieren. In Gegenwart von Wasser zersetzt es sich teilweise zu Chlorwasserstoff (Salzsäure). In wässriger Lösung ist AlCl3 vollständig ionisiert und die Lösung ist ein guter Leiter. Die Lösung ist sauer. Vereinfacht ausgedrückt kann das durch die Zersetzung von Aluminiumchlorid gebildete Kation wie folgt geschrieben werden:
- [Al(H 2 O) 6 ] 3 + + H 2 O ↽ – – ⇀ [Al(H 2 O) 5 OH] 2 + + H 3 O + .
AlCl3 ist wahrscheinlich die häufigste Lewis-Säure und eine der stärksten . Diese Verbindung findet breite Anwendung in der chemischen Industrie, insbesondere als Katalysator für Friedel-Crafts-Reaktionen (Alkylierung und Acylierung). Es wird auch bei Polymerisations- oder Isomerisierungsreaktionen organischer Verbindungen verwendet.
Es gibt auch Aluminiumchlorid (AlCl), aber es ist sehr instabil und kommt nur im gasförmigen Zustand vor.
Physikalische und chemische Eigenschaften von Aluminiumchlorid
Im festen Zustand kristallisiert Aluminiumchlorid mit der typischen YCl3-Struktur, wobei die Al3 + -Ionen ein kubisch-flächenzentriertes Gitter bilden.
Aluminiumchlorid ist eine starke Lewis-Säure. In Lewis-Säure-Base-Reaktionen kann es mit schwachen Lewis-Basen wie Benzophenon oder Mesitylen reagieren. In Gegenwart von Chloridionen reagiert es zu AlCl4- .
Bei der teilweisen Zersetzung in Gegenwart von Wasser entsteht Chlorwasserstoff und/oder Salzsäure. Wässrige Lösungen von Aluminiumchlorid verhalten sich ähnlich wie andere Salzlösungen, die wässrige Al3+ -Ionen enthalten . Beispielsweise bildet sich beim Mischen mit einer entsprechenden Menge Soda ein kolloidaler Niederschlag aus Aluminiumhydroxid:
- AlCl3 ( wässrig) + 3NaOH (wässrig) → Al(OH) 3 (s) + 3NaCl (wässrig) .
Kristallstruktur von Aluminiumchlorid
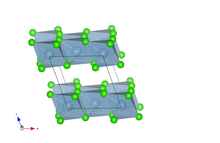
Im festen Zustand kristallisiert Aluminiumchlorid in Form einer monoklinen Struktur vom Typ RhCl3 mit der Raumgruppe C2/ m6 . Die Gitterparameter sind a = 5,914 Å , b = 10,234 Å und c = 6,148 Å , mit β = 108,25°. Auf dem Gitter nimmt Aluminium die Wyckoff-Position 4g ( y = 0,166) ein und Chlor die Positionen 4i ( x = 0,215 und z = 0,226) und 8j ( x = 0,252, y = 0,321, z = 0,225). Die resultierende Struktur ist eine Schichtstruktur in der (A, C)-Ebene mit Aluminium im Zentrum des Aluminiumoktaeders und einer Wabenstruktur in der (A, B)-Ebene.

Herstellung von Aluminiumchlorid
Aluminiumchlorid wird industriell durch eine direkte Reaktion zwischen Aluminium und Chlor hergestellt:
- 2Al + 3Cl2 → 2AlCl3
Oder aus Aluminium und Salzsäure:
- 2 Al + 6 HCl → 2 AlCl3 + 3 H2 .
Die Reaktion war exotherm und erforderte das Kühlen des Kolbens in einem kalten Wasserbad.
Die Passivierungsschicht des Aluminiums, bestehend aus Aluminiumoxid (Al2O3) , macht es zunächst weniger reaktiv, nach dem Entfernen dieser Schicht wird das Aluminium jedoch reaktiver . Daher wird empfohlen, das Aluminium mit 23 % konzentrierter Salzsäure zu ätzen und die Säure nach Beginn der Reaktion mit destilliertem Wasser zu verdünnen (um ihre Konzentration auf die Hälfte zu reduzieren), um die lokale (oberflächliche) Erwärmung zu begrenzen. Aluminium kann (trotz der allgemeinen Kühlung des Reaktionsmediums mit einem kalten Wasserbad) die Salzsäurelösung immer noch vergasen und gasförmigen Chlorwasserstoff freisetzen.
Der Ballon sollte auch deshalb geöffnet werden, weil, wie oben erwähnt, bei dieser Reaktion Wasserstoff freigesetzt wird. Es ist jedoch wünschenswert, die Entwicklung von Chlorwasserstoff zu begrenzen (Wasserdampf kondensiert an der Oberfläche des Trichters, und der größte Teil des beim Erhitzen der Salzsäure freigesetzten Chlorwasserstoffgases löst sich in den Wassertropfen und bildet erneut Salzsäure, die in das Reaktionsmedium zurückgeführt wird, wodurch Wasserstoff (und eine kleine Menge Chlorwasserstoff) durch die Löcher im Trichter entweichen können).
Anwendungen von Aluminiumchlorid
- Aluminiumchlorid wird hauptsächlich bei der Herstellung von Verbindungen über die von ihm katalysierte Friedel-Crafts-Reaktion verwendet, beispielsweise bei der Herstellung von Anthrachinon aus Benzol und Phosgen (wird in der Farbstoffindustrie verwendet ) . Bei der Friedel-Crafts-Reaktion reagiert ein Acylchlorid oder Alkylhalogenid mit einer aromatischen Verbindung:

Im Vergleich zu Benzolderivaten ist das Hauptreaktionsprodukt das Para -Isomer. Die Alkylierung gilt als weniger vorteilhaft als die Acylierung, da sie mit einer Reihe von Problemen verbunden ist. In jedem Fall ist das Aluminiumchlorid (bzw. die verwendete Apparatur) nicht völlig wasserfrei und für die Reaktion werden Spuren von Wasser benötigt . Eines der Probleme bei der Friedel-Crafts-Reaktion besteht darin, dass der Katalysator (Aluminiumchlorid) in stöchiometrischen Mengen vorhanden sein muss, damit die Reaktion vollständig abläuft, da dies die Bildung eines stabilen Komplexes mit dem Produkt erschwert.
Da sie recycelbar sind, müssen sie nach Gebrauch recycelt werden, was zu großen Mengen ätzender Abwässer führt. Zu diesem Zweck untersuchen Chemiker die Möglichkeit, umweltfreundlichere neutrale Katalysatoren wie Ytterbiumtriflat oder Dysprosiumtriflat zu verwenden. (Drittens) Der Preis ist relativ hoch, aber das Material ist recycelbar.
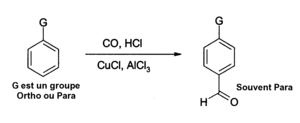
- Aluminiumchlorid kann auch verwendet werden, um Aldehydgruppen in aromatische Ringe einzuführen, beispielsweise in der Gattermann-Koch-Reaktion mit Kohlenmonoxid, Chlorwasserstoff und Kupfer(I)-chlorid als Cokatalysatoren:
- Aluminiumchlorid hat viele weitere Verwendungsmöglichkeiten in der organischen Chemie:
- AlCl3 wird bei Polymerisations- oder Isomerisierungsreaktionen organischer Verbindungen verwendet . Wichtige Anwendungen sind die Herstellung von Ethylbenzol (zur Verwendung bei der Herstellung von Styrol und Polystyrol) und die Herstellung von Dodecylbenzol (zur Verwendung bei der Herstellung von Aluminiumchlorid-Reinigungsmitteln).
- AlCl3 eignet sich besonders gut als Katalysator für die Diels-Alder-Reaktion.
- – ButenAlCl3 kann auch die Additionsreaktion von 2-3-Ketonen mit Carotinoiden katalysieren:

- Schließlich handelt es sich um ein anorganisches Koagulans, das in Form von Polyaluminiumchlorid (PAC) 7 in einigen Wasseraufbereitungsprozessen weit verbreitet ist. Es entfernt auch überschüssiges Fluorid aus dem Wasser. Um eine Verunreinigung des Trinkwassers mit Aluminium zu vermeiden und gute Koagulationsergebnisse zu erzielen, ist eine sorgfältige Kontrolle des pH-Werts des Koagulationsprozesses und der verwendeten Dosierung erforderlich. 7. Wassermisch- und Filtersysteme (zum Entfernen von Aluminiumklumpen) müssen ausreichend sein. 7 . Chitosan und Bentonit sind nützliche Zusatzstoffe 7.

Bersa-Produktverpackung
Sicherheit von Aluminiumchlorid
AlCl3 kann bei Kontakt mit Alkali oder Wasser eine Explosion verursachen . Da es sich um ein Reagenz handelt, ist beim Arbeiten mit Aluminiumchlorid Vorsicht geboten und es sollten Schutzhandschuhe und eine Schutzbrille getragen werden. Das Dämpfen sollte unter einer Abzugshaube erfolgen. Bei Verwendung in feuchtem Klima nimmt Aluminiumchlorid schnell Feuchtigkeit auf, wird stark sauer und korrodiert schnell eine Vielzahl von Materialien, darunter Edelstahl und Gummi.
Aluminiumchlorid-Hexahydrat
Strukturformel: AlCl3 ( H2O ) 6 .
Dieses Produkt ist von Natur aus stabil und verursacht keine Hautreizungen. Es wird auch in Hautpflegeprodukten verwendet ( siehe Hyperhidrose).
Dies ist die häufigste Form der Herstellung von Aluminiumchlorid, bei der das wasserfreie Salz nicht benötigt wird. Seine CAS-Nummer lautet 7784-13-6. Seine Molmasse beträgt 241,432 g /mol .
Hauptsynonyme:
- Englischer Name: Aluminiumtrichlorid-Hexahydrat;
- Englischer Name: Aluminiumtrichlorid-Hexahydrat.


![{\displaystyle {\ce {[Al(H2O)6]^3+ + H2O <=> [Al(H2O)5OH]^2+ + H3O+}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ca99634e7b52aac56a62d879a5eccde92f41ea87)